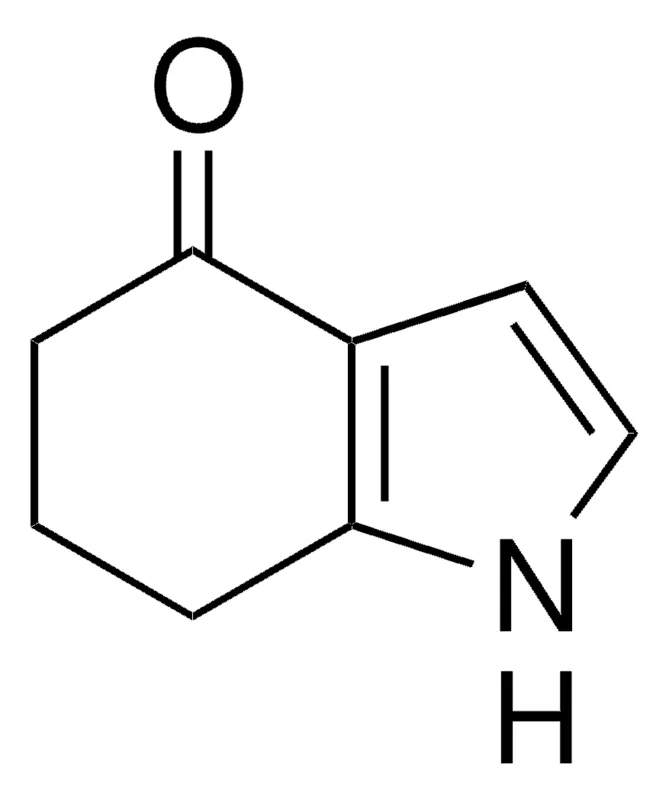
1,5,6,7-Тетрагидро-4H-индол-4-он
2 231,00 ₽
1,5,6,7-Тетрагидро-4H-индол-4-он 98% (CAS 13754-86-4) — ключевой полупродукт в синтезе биоактивных соединений. Применяется НПО ЭкоТек в фармацевтике.
Описание:
1,5,6,7-Тетрагидро-4H-индол-4-он представляет собой органическое соединение класса индолов, являющееся ключевым полупродуктом в органическом синтезе. Йодирование этого соединения с использованием 1-хлорметил-4-фтор-1,4-диазониабицикло[2.2.2]октан бис(тетрафторбората) приводит к образованию α-йодопроизводного в качестве основного продукта. Соединение проявляет высокую реакционную способность за счет кетонной группы и ароматического фрагмента, что позволяет использовать его в синтезе сложных гетероциклических систем. Обладает кристаллической структурой, растворимо в полярных органических растворителях, таких как диметилформамид и ацетонитрил. Применяется НПО ЭкоТек в разработке фармацевтических субстанций.
Применение:
1,5,6,7-Тетрагидро-4H-индол-4-он широко применяется НПО ЭкоТек как многофункциональный реагент в синтезе биологически активных соединений: 1. Производство 4-оксо-4,5,6,7-тетрагидро-1H-индол-2-карбонитрила, метил-2-(4-оксо-4,5,6,7-тетрагидро-1H-индол-1-ил)акрилата и 3-(4-оксо-4,5,6,7-тетрагидро-1H-индол-1-ил)пропаннитрила. 2. Синтез мощных и перорально активных агонистов 5-HT1A рецепторов: (R)-(+)- и (S)-(-)-1-формил-6,7,8,9-тетрагидро-N,N-дипропил-3H-бенз[e]индол-8-аминов. 3. Получение противоопухолевого агента псаммопеммина A. 4. Производство 1,3,4,5-тетрагидробензиндольных β-кетоэфиров и трициклических тетрагидробензиндолов через реакции C-H-инсерции. 5. Создание ингибиторов гуанилатциклазы — трициклических индольных и дигидроиндольных производных. 6. Получение конденсированных пирролоиндолов посредством Pd-катализируемой внутримолекулярной функционализации C-H связи (галогенбензил)пирролов. 7. Энантиоселективный синтез арилалкенилиндолов через асимметричную C-H-инсерцию карбеноидов родия с последующей перегруппировкой Копе и элиминированием.
Похожие товары
Химические строительные блоки
Химические строительные блоки
Химические строительные блоки
4-Броманилин 97%: ключевой интермедиат для нанотрубок и синтеза
Химические строительные блоки
Химические строительные блоки
Химические строительные блоки
Химические строительные блоки
Химические строительные блоки