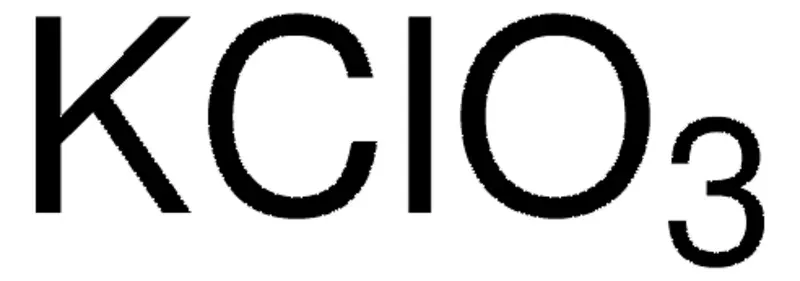Хлорат калия 99-101% для синтеза оксида графита
8 180,00 ₽
Хлорат калия KClO₃ с чистотой 99-101% для синтеза оксида графита и пиротехники. Кристаллическая форма. Опт и розница от НПО ЭкоТек.
Описание:
Кристаллы хлората калия (KClO₃) относятся к моноклинной сингонии. При нагревании выше 400°C вещество разлагается с образованием хлорида калия (KCl) и перхлората калия (KClO₄). Обладает сильными окислительными свойствами. Под воздействием рентгеновского излучения на обогащенном кислородом-17 KClO₃ образуется радикал O₃⁻, исследованный методом ЭПР (электронного парамагнитного резонанса). Облучение хлората калия рентгеновскими лучами вызывает разложение с образованием хлорида, хлорита, гипохлорита и окклюдированного кислорода. Также образуются значительные количества гексаоксида дихлора (Cl₂O₆) и следовые количества диоксида хлора (ClO₂). Хлорат калия находит применение в пиротехнике, производстве спичек, как источник кислорода в лабораторных условиях и компонент взрывчатых составов. Требует осторожного обращения из-за высокой реакционной способности. При хранении следует избегать контакта с восстановителями и источниками тепла.
Применение:
Хлорат калия может использоваться для приготовления оксида графита (GO) в лабораторных условиях. Также применяется в пиротехнических составах, производстве спичек и как окислитель в химических синтезах. В фармацевтической промышленности служит антисептиком, а в сельском хозяйстве — дефолиантом. Важно соблюдать меры безопасности при работе с этим сильным окислителем.
Похожие товары
Лабораторные химикаты
Лабораторные химикаты
Катализаторы для GMP
Алюминиевый порошок ЭкоТек Пиротехнический ≥91% (CAS 7429-90-5, металлургия, химия)
Лабораторные химикаты
Лабораторные химикаты
Лабораторные химикаты
Лабораторные химикаты
Лабораторные химикаты