Ингибитор IRE1 III, 4μ8C
10 674,00 ₽
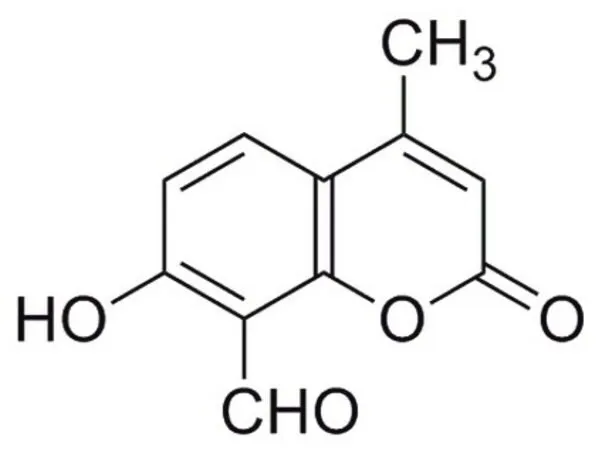
Ингибитор IRE1 III, 4μ8C: селективный ковалентный ингибитор РНКазы IRE1α (IC50 до 45 нМ). Блокирует ER-стресс-индуцированный сплайсинг XBP1 и деградацию мРНК. Купить ≥95% (ВЭЖХ) в НПО ЭкоТек.
Описание:
Ингибитор IRE1 III, 4μ8C — это клеточно-проницаемое соединение класса кумаринов, обладающее структурой о-гидроксиальдегида. Он избирательно подавляет РНКазную активность IRE1 (инозит-требующего фермента 1) по ковалентному механизму, формируя основание Шиффа с лизином-907 в активном центре фермента. Ингибирование проявляет зависимость от времени и концентрации: IC50 составляет 550, 230, 180, 100 и 45 нМ при предынкубации 0, 2, 4, 8 и 16 минут соответственно (по данным FRET-анализа расщепления РНК). Эффективно блокирует индуцированный стрессом эндоплазматического ретикулума (ЭР) сайт-специфический сплайсинг мРНК, а также RIDD-зависимую деградацию мРНК (IC50 = 6.9 и 4.1 мкМ для сплайсинга Xbp1 и деградации Scara3 соответственно) в культурах эмбриональных фибробластов мыши после обработки туникамицином. В клетках опухолевой ацинарной поджелудочной железы крысы AR42J ингибирует индуцированное дексаметазоном расширение емкости ЭР (эффективная концентрация 32 мкМ) и секрецию амилазы (IC50<2 мкМ). Структурный анализ показал, что ограниченный доступ воды к Lys907 в нативной конформации IRE1 объясняет необычную стабильность основания Шиффа и лежит в основе селективности ингибирования. Хотя 4μ8C также способен ингибировать аутофосфорилирование IRE1, взаимодействуя с Lys599, внутриклеточные нуклеотиды предотвращают этот процесс в физиологических условиях. Селективность и механизм действия делают 4μ8C ценным инструментом для изучения сигнального пути UPR (развернутый белковый ответ) и разработки терапевтических стратегий при заболеваниях, связанных с дисфункцией ЭР. Применяется в исследованиях нейродегенеративных заболеваний, диабета, воспаления и рака.
Применение:
Ингибитор IRE1 III, 4μ8C применяется в фундаментальных и прикладных исследованиях для модуляции сигнального пути UPR (развернутый белковый ответ) в эндоплазматическом ретикулуме. Основные направления: изучение механизмов ER-стресса при нейродегенеративных заболеваниях (болезнь Альцгеймера, Паркинсона), диабете, воспалительных процессах и онкологии. Используется в экспериментах на клеточных культурах (включая MEF и линии раковых клеток) для ингибирования сайт-специфического сплайсинга мРНК XBP1 и RIDD-зависимой деградации транскриптов. Эффективен в моделях с индукторами ER-стресса (туникамицин, дексаметазон). Позволяет исследовать роль IRE1 в секреторных процессах (например, подавление секреции амилазы в панкреатических ацинарных клетках), апоптозе и адаптационных реакциях клетки. Благодаря высокой селективности к РНКазному домену IRE1, является перспективным фармакологическим инструментом для разработки таргетной терапии.
Похожие товары
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Биохимические реактивы
Биоактивные малые молекулы