Антитело к IgG мыши (Fc-специфичное) – биотин
13 032,00 ₽
Антитело к IgG мыши (Fc-специфичное) – биотин, полученное из козы, аффинно-выделенное, забуференный водный раствор. Производство: НПО ЭкоТек.
Описание:
IgG присутствует в больших количествах в сыворотке человека, составляя около 10-20% белков плазмы. Это гликопротеин, содержащий 82-96% белков и 4-18% углеводов. IgG подразделяется на четыре подкласса: IgG1, IgG2, IgG3 и IgG4. Молекула IgG состоит из четырех полипептидных цепей: двух тяжелых цепей (γ-цепи) и двух легких цепей (κ или λ), соединенных дисульфидными связями. Тяжелая цепь содержит N-концевой вариабельный домен (VH) и три константных домена (CH1, CH2, CH3), между CH1 и CH2 находится шарнирная область. Легкая цепь состоит из вариабельного домена (VL) и константного домена (CL). Антигенсвязывающий фрагмент (Fab) образуется за счет соединения VH и CH1 с VL и CL. Молекулярная масса IgG составляет около 150 кДа. Данное антитело специфично к Fc-фрагменту мышиного IgG, что позволяет избежать перекрестной реактивности с Fab-фрагментами. Конъюгация с биотином обеспечивает высокое сродство к авидину и стрептавидину, что делает его эффективным инструментом в иммуноферментном анализе (ELISA), иммуноблоттинге, иммуногистохимии и других методах. Биотиновая метка стабильна и обеспечивает усиление сигнала при использовании стрептавидин-ферментных комплексов.
Применение:
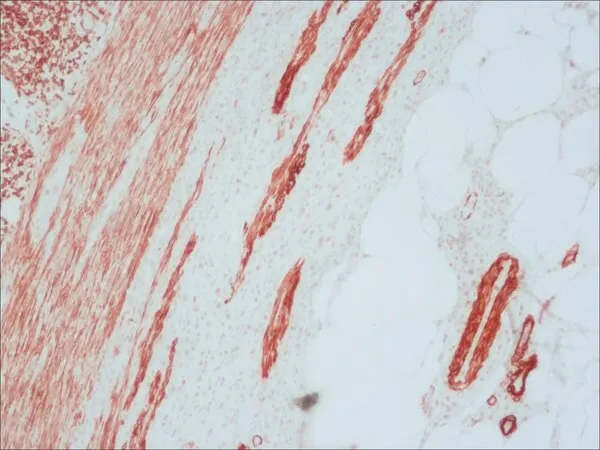
Антитело к IgG мыши (Fc-специфичное), меченное биотином, применяется в иммуноферментном анализе (ELISA), дот-блоттинге, иммуногистохимии, ядерном мечении, методе ингибирования ELISA и иммуноцитохимии. В частности, оно использовалось для визуализации неонатального миозина в срезах мышц цыпленка и для ELISPOT-анализа уровней IgG у мышей, инфицированных холерным токсином.
Похожие товары
Протеиновая биология
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Биоактивные малые молекулы
Протеиновая биология
Разное
Биоактивные малые молекулы